美国食品药品监督管理局 (FDA) 已授予 rezpegaldesleukin 快速通道资格,用于治疗成人和 12 岁及以上、体重至少 40 公斤的儿科患者的重度至极重度斑秃。 Rezpegaldesleukin 是一款在研生物制剂
美国食品药品监督管理局 (FDA) 已授予 rezpegaldesleukin 快速通道资格,用于治疗成人和 12 岁及以上、体重至少 40 公斤的儿科患者的重度至极重度斑秃。
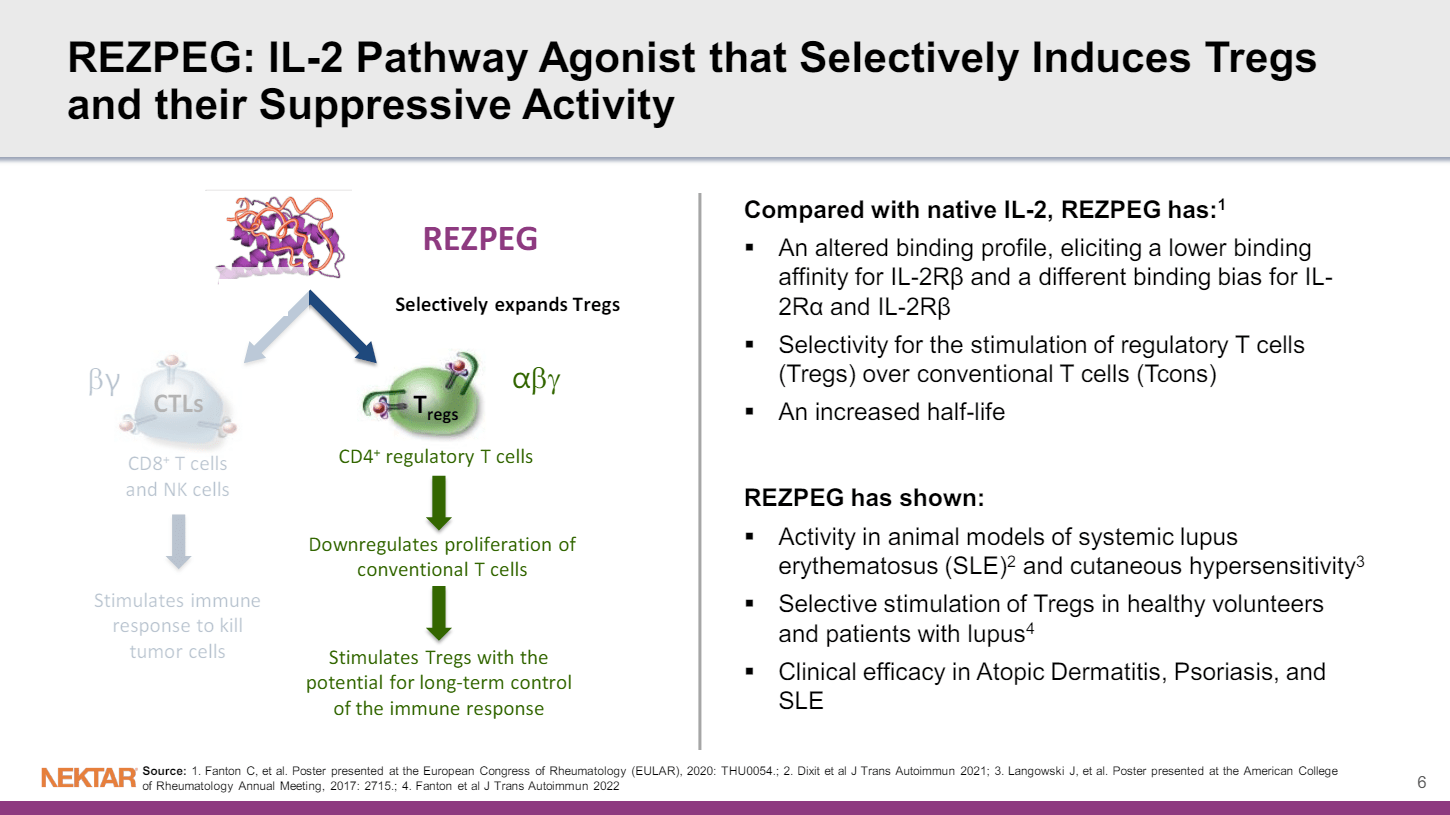
Rezpegaldesleukin 是一款在研生物制剂,旨在通过靶向白细胞介素-2受体复合物,刺激调节性T细胞 (Treg) 增殖,从而恢复自身免疫性和炎症性疾病患者的免疫系统稳态。Rezpegaldesleukin 获得快速通道资格认定是基于研究数据,该数据表明,使用 Rezpegaldesleukin 治疗的其他炎症性皮肤病患者的 Treg 细胞有所增加。
目前正在开展一项名为 REZOLVE-AA 的 2b 期临床试验(ClinicalTrials.gov 标识符: NCT06340360 ) ,以评估 rezpegaldesleukin 的安全性和有效性。该试验针对重度至极重度斑秃(头皮受累≥50%)患者,且此前未接受过 Janus 激酶 (JAK) 抑制剂或其他生物制剂治疗。该研究预计将入组约 90 名患者。
研究参与者将被随机分配接受每两周一次皮下注射瑞兹佩加地白介素(低剂量或高剂量)或安慰剂。主要终点是第36周脱发严重程度工具 (SALT) 评分相对于基线的平均变化百分比。次要终点包括其他时间点SALT评分相对于基线的平均变化百分比、SALT评分降低至少50%的患者比例以及达到SALT-20(绝对SALT评分≤20)的患者比例。
Nektar Therapeutics 预计将于 2025 年 12 月公布 REZOLVE-AA 试验的顶线数据。Rezpegaldesleukin 也正在对中度至重度特应性皮炎患者进行评估(ClinicalTrials.gov 标识符:NCT06136741),并且也获得了该适应症的快速通道资格。
Nektar Therapeutics receives Fast Track designation for rezpegaldesleukin for the treatment of severe-to-very severe alopecia areata. News release. Nektar Therapeutics.
温馨提示:以上资讯由香港登越药业整理编辑(如有错漏,请帮忙指正),提供全球最新上市药品的资讯,具体用药指引,请咨询主治医师。
(责任编辑:登越药房)




