美国食品药品监督管理局 (FDA) 已对 durvalumab 用于治疗可切除、早期和局部晚期 (II-IVA 期) 胃癌和胃食管连接部 (GEJ) 癌患者的治疗给予优先审查。 Durvalumab 是一种程序性死亡配体 1 (PD-L
美国食品药品监督管理局 (FDA) 已对 durvalumab 用于治疗可切除、早期和局部晚期 (II-IVA 期) 胃癌和胃食管连接部 (GEJ) 癌患者的治疗给予优先审查。
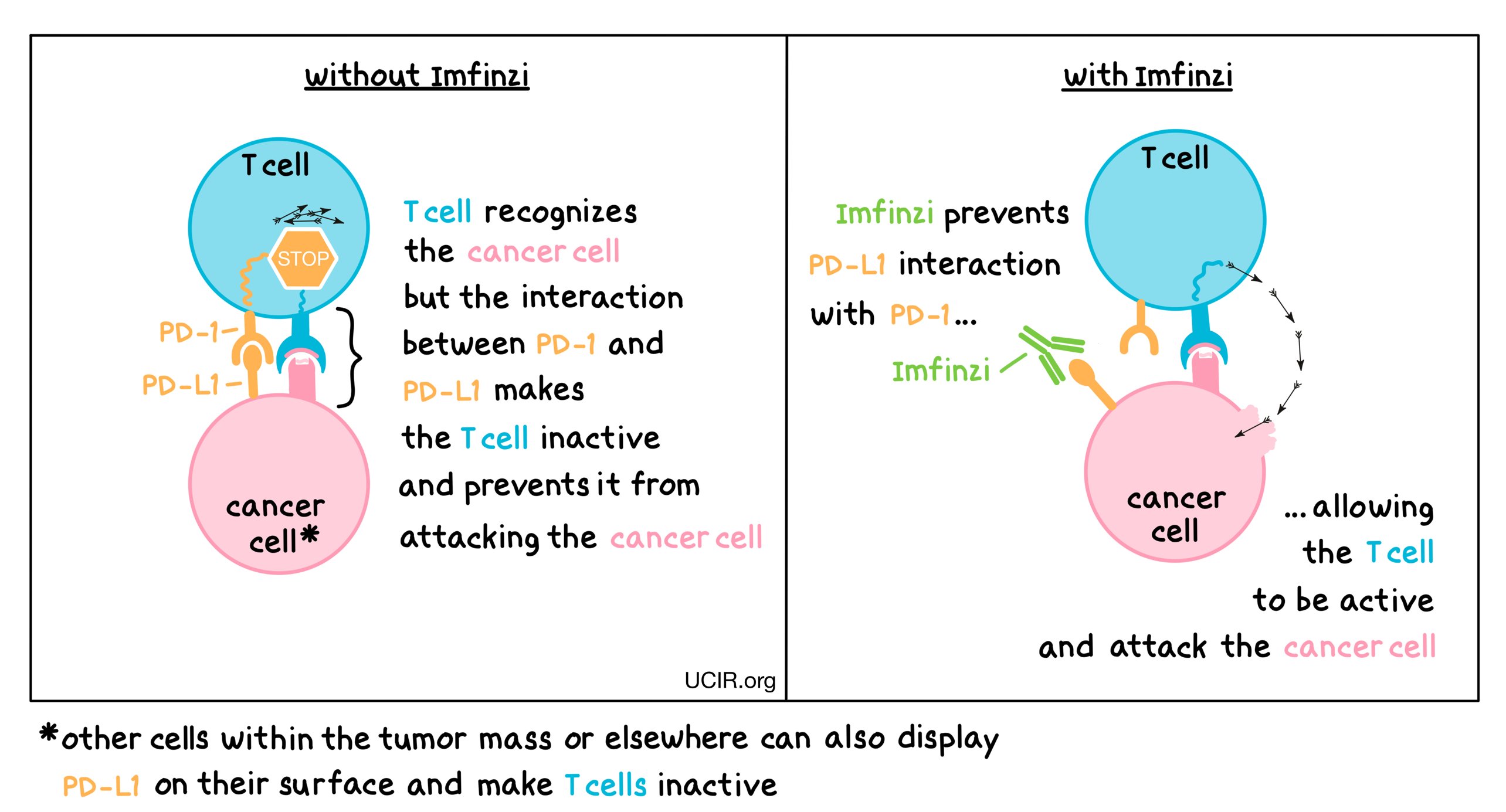
Durvalumab 是一种程序性死亡配体 1 (PD-L1) 阻断抗体,目前已获批,商品名为Imfinzi® ,用于治疗非小细胞肺癌、小细胞肺癌、胆道癌、肝细胞癌、子宫内膜癌和肌层浸润性膀胱癌。该药物用于胃癌/GEJ 癌适应症的补充生物制品许可申请 (Biologics License Application) 已获得双盲、安慰剂对照的 MATTERHORN 试验(ClinicalTrials.gov 标识符:NCT04592913)的数据支持。
研究中,948 名参与者被随机分配接受度伐利尤单抗或安慰剂治疗,并在手术前每 4 周接受一次 FLOT(氟尿嘧啶、亚叶酸钙、奥沙利铂和多西他赛)化疗,共 2 个周期。手术后,每 4 周接受一次度伐利尤单抗或安慰剂治疗,共 12 个周期(包括 2 个周期的度伐利尤单抗或安慰剂联合 FLOT 化疗,以及 10 个周期的度伐利尤单抗或安慰剂单药治疗)。试验的主要终点是无事件生存期 (EFS)。
计划中的中期分析结果显示,该研究已达到其主要终点,即与安慰剂方案相比,durvalumab方案在EFS方面取得了具有统计学意义和临床意义的改善(风险比[HR],0.71% [95% CI, 0.58-0.86];P < .001)。durvalumab组尚未达到中位EFS,对照组为32.8个月。
1年后,接受基于度伐利尤单抗的围手术期方案的患者中,78.2%的患者无事件发生,而对照组中该比例为74.0%;24个月时的预计无事件生存率分别为67.4%和58.5%。虽然中期分析未达到总生存率(次要终点),但观察到度伐利尤单抗具有良好的治疗趋势(HR,0.78 [95% CI,0.62-0.97];P = 0.025);最终分析结果将进一步评估。
阿斯利康肿瘤血液学研发执行副总裁Susan Galbraith表示:“此次优先审评强化了Imfinzi在围手术期治疗中改变早期胃癌和胃食管交界处癌患者治疗方案的潜力,这些患者即使在接受根治性手术和围手术期化疗后也常常面临疾病复发或进展。这种新型疗法是唯一一种基于免疫疗法的方案,在此类患者中显示出显著降低疾病进展、复发或死亡风险的统计学意义,如果获得批准,将有望改变临床治疗模式。”
预计将于 2025 年第四季度对胃癌/GEJ 癌适应症做出监管决定。FDA 还授予 durvalumab 在此情况下的突破性疗法认定。
参考来源:Imfinzi® (durvalumab) granted Priority Review and Breakthrough Therapy Designation in the US for patients with resectable early-stage gastric and gastroesophageal junction cancers. News release. AstraZeneca.
温馨提示:以上资讯由香港登越药业整理编辑(如有错漏,请帮忙指正),提供全球最新上市药品的资讯,具体用药指引,请咨询主治医师。
(责任编辑:登越药房)




